中商情報網訊:優先審批程序是指根據申請人的請求,對納入優先審批程序的醫療器械產品,在注冊申請前及審評審批過程中,設立特別通道,優先進行服務的程序。其主要為治療罕見病、惡性腫瘤、老年病、兒童專用、臨床急需以及列入國家科技重大專項或重點研發計劃等情形的醫療器械產品設置優先審批通道。根據眾成醫械大數據平臺統計,2020年全國醫療器械進入優先審批通道數量達237件,較去年同期(180件)增長31.67%。
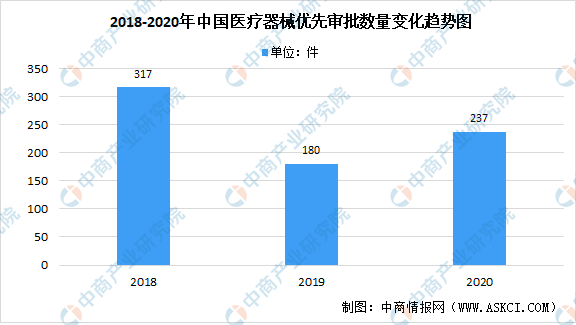
數據來源:眾成醫械、中商產業研究院整理
1.省級排名
從全國各省醫療器械優先審批數量分布來看,廣東省以265件高居第一位,天津市以257件居第二位,重慶市以121件居第三位。其后分別是安徽省、福建省、山東省、上海市、北京市、浙江省、湖北省。
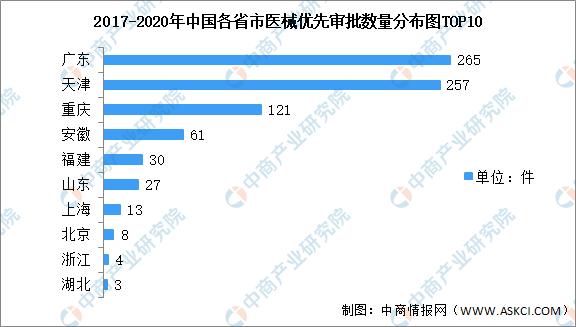
數據來源:眾成醫械、中商產業研究院整理
2018年8月8日,《廣東省食品藥品監督管理局第二類醫療器械優先審批程序》經廣東省人民政府法制辦公室審查通過,自2018年10月1日起施行。該政策主要修訂內容之一:保留質量信用A類企業的原激勵措施,提供專門的注冊申報通道,不再需要企業提出優先審批申請、等待網上公示及獲取通知單。這是導致廣東省265件醫療器械優先審批產品中224件(約占84.53%)是政策獎勵的直接原因。
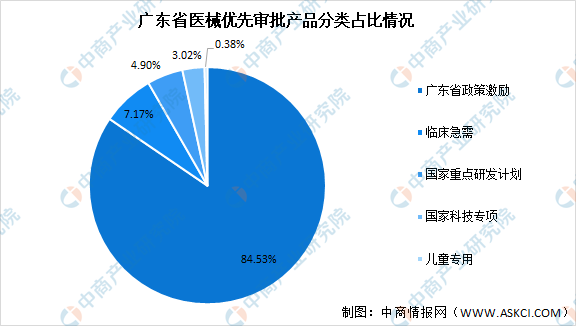
數據來源:眾成醫械、中商產業研究院整理
2.市級排名
從全國各市醫療器械優先審批數量分布來看,深圳市以109件高居第一位,廣州市以69件居第二位,合肥市以44件居第三位。其后分別是珠海市、東莞市、淄博市、福州市、廈門市、揭陽市、蕪湖市。
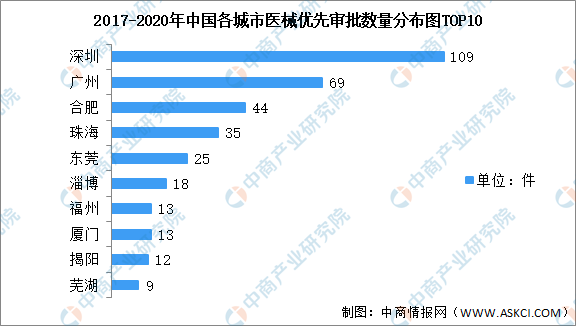
數據來源:眾成醫械、中商產業研究院整理
隨著我國社會和科技發展、疾病診療水平和人們生活水平不斷的提高,越來越多具有突破性和創新性的醫療器械涌現,以滿足多樣化的疾病診療需求。為支持和鼓勵優質醫療器械的注冊上市,2016年國家出臺《醫療器械優先審批程序》,該政策大力支持罕見病、老年人特有和多發疾病及臨床急需器械的發展,加快其上市進程。隨后,各個省市相繼出臺《第二類醫療器械優先審批程序》,激勵許多醫療器械產品進入優先審批通道。未來,在政策的激勵和企業的大力支持下,醫療器械優先審產品數量有望進一步增加。
更多資料請參考中商產業研究院發布的《2021年“十四五”中國醫療器械行業市場前景及投資研究報告》,同時中商產業研究院還提供產業大數據、產業情報、產業研究報告、產業規劃、園區規劃、十四五規劃、產業招商引資等服務。
 如發現本站文章存在版權問題,煩請聯系editor@askci.com我們將及時溝通與處理。
如發現本站文章存在版權問題,煩請聯系editor@askci.com我們將及時溝通與處理。

