中商情報網訊:隨著全球醫藥市場競爭的日益激烈,藥企對于研發、生產、銷售成本的控制和效率的提升需求強烈催生了醫藥外包行業的產生。醫藥外包行業又逐漸分化為專業的研發外包(CRO)、生產外包(CMO)、臨床試驗現場管理外包(SMO)等。數據顯示,SMO行業市場規模從2018年的23.3億元增長至2019年的33.6億元,同比增長44.2%。,預計在2022年將進一步增長至100.4億元,2019年至2022年復合年增長率44.0%。
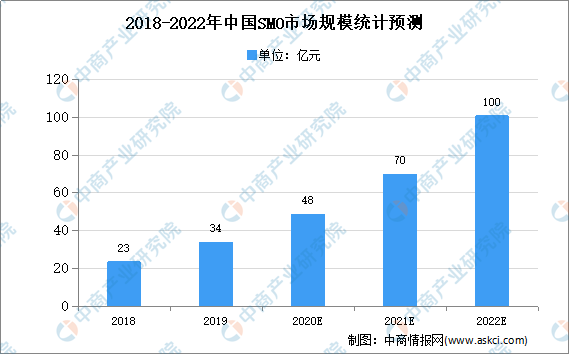
數據來源:尚普、中商產業研究院整理
人員規模持續增長,行業處于快速發展期
隨著國內臨床試驗機構數量的不斷增長,臨床試驗機構分布的城市數量也隨之增加。為了實現對臨床試驗機構的覆蓋,需要SMO企業向臨床試驗所在城市或臨近城市派駐更多CRC(臨床研究協調員)人員,因此CRC人員規模也是衡量SMO企業服務能力的重要指標之一。近年來國內CRC人員數量迅速增長,SMO行業處于快速發展期。
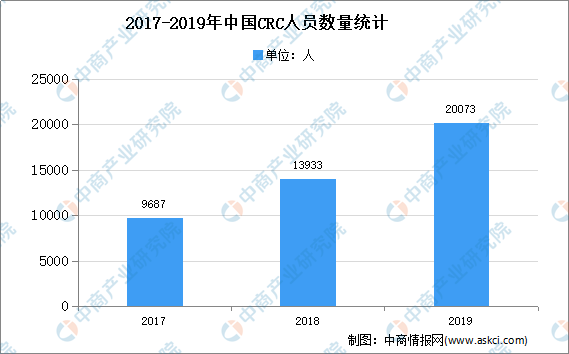
數據來源:尚普、中商產業研究院整理
服務周期較長
藥物從研究開始到上市銷售是一項高技術、高風險、高投入和長周期的復雜系統工程,以化學藥為例,主要研究與開發工作包括化合物研究、臨床前研究、臨床試驗申請與批準、臨床研究、藥品注冊申請與審批以及上市后持續研究。臨床研究時間周期可能長達10年,整個過程不可預見因素較多,因此,大多數制藥企業會選擇將藥物研發部分或全部委托給CRO公司,并且越來越多的制藥企業將臨床試驗現場管理委托給SMO公司。
人員區域發展不平衡進一步改善
受到各地區臨床試驗數量的影響,全國擁有CRC人員的城市中,北京、上海、廣州等一線城市人數規模占有絕對優勢,反映了我國CRC人員分布區域差異化的現狀。另一方面,隨著新藥臨床試驗正在向二、三線城市加快發展,近年來二、三線城市的CRC絕對數量呈明顯上升趨勢。根據中國CRC之家不完全統計,全國CRC人員分布城市由2014年61個城市增長至2019年179個城市,區域發展不均衡的狀況正在改善。
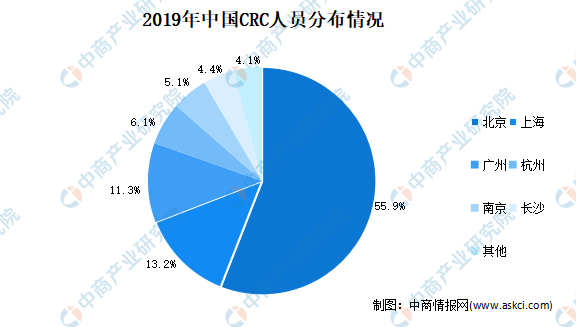
數據來源:尚普、中商產業研究院整理
多中心臨床試驗帶動行業發展
目前,中國臨床試驗正處在高速變革的階段。《關于深化審評審批制度改革鼓勵藥品醫療器械創新的意見》,重點指出“改革臨床試驗管理,加快上市審批速度”。在放寬臨床試驗中心資格認定標準,鼓勵醫療機構、醫學研究機構、醫藥高等學校開展臨床試驗的同時,提高了對臨床試驗質量的要求。意見中還提出,允許境外企業和科研機構在我國依法同步開展國際多中心臨床試驗,及接受境外臨床試驗數據。該意見的發布,為在我國開展多中心臨床試驗和參與國際多中心臨床試驗創造了前所未有的發展契機。
SMO企業的管理體系和資源愈發受到重視
項目管理能力、項目執行經驗及臨床試驗機構覆蓋能力是項目申辦方選擇SMO企業主要的衡量標準之一。臨床試驗項目的設計越來越復雜,項目的組織、管理拆分也越來越細。通過建立有效的項目管理體系將繁瑣的事務性工作流程化、分解化、高效化,形成標準化操作流程,可使所有參與臨床試驗的機構的執行人員處于同一個技術質量水平上,繼而推進試驗進度和質量。具備完善項目管理體系的SMO企業可將標準的操作流程,快速復制到其他臨床試驗項目,提高臨床試驗項目的效率。
更多資料請參考中商產業研究院發布的《中國SMO行業市場前景及投資機會研究報告》,同時中商產業研究院還提供產業大數據、產業情報、產業研究報告、產業規劃、園區規劃、十四五規劃、產業招商引資等服務。
 如發現本站文章存在版權問題,煩請聯系editor@askci.com我們將及時溝通與處理。
如發現本站文章存在版權問題,煩請聯系editor@askci.com我們將及時溝通與處理。

