中商情報網訊:3月11日,國家衛健委發布《新冠病毒抗原檢測應用方案(試行)》通知,首次明確了新冠病毒抗原自測的相關政策,社區居民有自我檢測需求的,可通過零售藥店、網絡銷售平臺等渠道,自行購買抗原檢測試劑進行自測。
3月11-12日,諾唯贊、北京金沃夫、深圳華大因源、萬孚生物、北京華科泰生物的新冠病毒抗原檢測試劑申請自測應用變更并獲得國家藥監局批準,原來作為“專業版”的新冠病毒抗原檢測試劑正式變更增加自測應用,可用于居民自我檢測。為了緩解新冠病毒抗原自測需求,3月13日,國家藥監局再次應急批準了另外5家新冠抗原自測產品的注冊申請,分別來自萬泰生物、熱景生物、天津博奧賽斯生物、重慶明道捷測生物和樂普診斷的5款“自測版”新冠病毒抗原檢測試劑。

資料來源:中商產業研究院整理
依據《體外診斷試劑分類規則》,新型冠狀病毒(2019-nCoV)抗原檢測試劑盒按照第三體外診斷試劑管理,分類編碼為6840,因此新冠病毒抗原自測試劑應按照第三類體外診斷試劑的要求,向國家藥監局申請注冊。目前,我國體外診斷市場規模從2016年的450億元增長到2019年的864億元,占醫療器械市場規模的比例從2016年的12.2%增長到2019年的13.9%。未來,預計體外診斷市場有望繼續保持增長,到2022年,我國體外診斷市場規模預計將達到1460億元,2019-2024年的年均復合增長率為17.8%,占醫療器械市場規模的比例將達到15.9%。
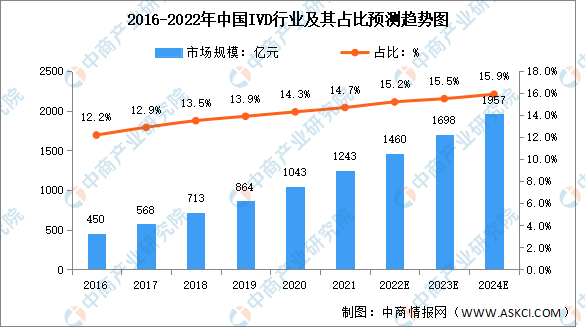
數據來源:弗若斯特沙利文、中商產業研究院整理
 如發現本站文章存在版權問題,煩請聯系editor@askci.com我們將及時溝通與處理。
如發現本站文章存在版權問題,煩請聯系editor@askci.com我們將及時溝通與處理。

